BIOFISICA | SILVA | S.ISIDRO-MI-SA:7-13hs 1 ° cuatr. 2026
| Tema | Nombre | Descripción |
|---|---|---|
| GUIAS DE EJERCICIOS | ||
| U1: Cinemática (MRUV) | Demostración de porqué en ausencia de aire todos los cuerpos caen con la misma aceleración. |
|
Ésta es la cámara de vacío más grande del mundo con 37 metros de altura y 30 de diámetro, capaz de absorber 700.00 litros de aire por segundo. Tiene dos puertas con un grosor de 2,5 metros que, una vez cerradas herméticamente, activan un sistema de turbinas que tardan tres horas en vaciar la mayor parte del aire. Se lanzan al mismo tiempo en esta sala distintos objetos, como una gran y pesada bola de bolos y unas ligeras plumas. El video está en inglés pero la contundencia de las imágenes exime de mayores comentarios para la interpretación del fenómeno. |
||
| U1: Dinámica | El movimiento de los cuerpos : Causas |
|
| U1: Trabajo y Energía | |
|
|
||
Bajen el siguiente archivo y podrán observar el movimiento de un patinador sobre una pista. Sobre el margen derecho observarán una serie de controles (seleccionen la opción "eliminar calor"). Experimenten modificando la pista, la aceleración de la gravedad, incluir el efecto de la fuerza de rozamiento, etc. Evaluén que sucede con las energías mecánica, potencial y cinética. Disponen de gráficos diversos. Esperamos que lo disfruten!! |
||
| U2: Hidrostática |
|
|
Bajen el archivo (formato power-point ejecutable, pps) y recréense con su contenido. Encontrarán desde el desarrollo de algunos ejercicios de la guía de trabajos prácticos hasta información que relaciona los principios físicos dictados en clase con las implicaciones en clínica médica a las que dichos principios orientan. Fundamentalmente veremos como el concepto de presión en los fluidos incide en aspectos relacionados con la respiración, la circulación sanguínea, el buceo, etc
|
||
|
||
| U2: Hidrodinámica de fluidos ideales |
Ecuación de la Continuidad - Teorema de Bernoulli |
|
| U2: Hidrodinámica de fluidos reales |
Ley de Ohm - Ley de Poiseuille |
|
Arreglos en serie y paralelo |
||
| Parciales para ejercitar (1º) | ||
| U3: Calorimetría | ||
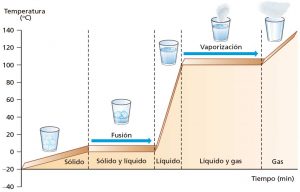
El punto de fusión es la temperatura a la que una sustancia en estado sólido se transforma en estado líquido. Por el contrario, el punto de solidificación, también conocido como punto de congelación, es la temperatura a la que un líquido se convierte en sólido. Y esto cambia en fusión de la presion atmosférica. En el siguiente diagrama de fases del agua, vemos por ejemplo que a 1 atmosfera, el punto de fusión (o de solidificación) es a 0 °C. El punto de ebullición es la temperatura a la que un líquido se convierte en gas, mientras que el punto de condensación es la temperatura a la que un gas se convierte en líquido. A 1 atmosfera, el punto de ebullición (o de condensación) e100 a 0 °C. El agua puede cambiar de estado (sólido, líquido, gaseoso) a través de diferentes procesos como la fusión (sólido a líquido), la solidificación (líquido a sólido), la vaporización (líquido a gaseoso), la condensación (gaseoso a líquido), la sublimación (sólido a gaseoso) y la de sublimación (gaseoso a sólido). El agua es el único componente de la Tierra que puede encontrarse en tres estados físicos: sólido, líquido y gaseoso.
El calor específico del agua es la cantidad de calor necesaria para elevar la temperatura de 1 gramo de agua en 1 grado Celsius. El calor latente del agua, por otro lado, es la cantidad de calor necesaria para cambiar el estado del agua de un estado a otro sin cambiar su temperatura. El calor específico del hielo es 0.5 cal/g·°C, el del agua es 1 cal/g·°C y el del vapor de agua es aproximadamente 0.48 cal/g·°C. Los cambios de estado se realizan a temperatura constante. Se necesitan 80 cal/g para derretir hielo (o congelarlo) y 540 cal/g para evaporar (o condensar). A lo largo de los cambios de estado, o transiciones de fases coexisten ambas fases, la materia en ambos estados.
|
||
equilibrio térmico |
||
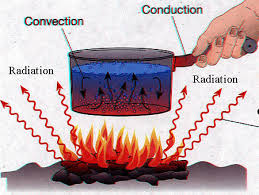
| U3: Transmisión del calor | Transmisión del calor
|
|
| U3: Primer Principio de la Termodinámica |
Primer principio de la termodinámica
|
|
Ejemplos de cálculo de trabajo en gases, sobre un diagrama p-V, para evoluciones reversibles |
||
Aplicación del primer principio de la termodinámica a una serie de evoluciones de un gas ideal (isobárica, isocórica e isotérmica) y al ciclo que las mismas constituyen. |
||
Nuevo ejemplo para una evolución entre dos estados de un gas ideal, utilizando para el cálculo de la variación de energía interna una expresión en función de las presiones y volumenes iniciales y finales. |
||
Dos evoluciones entre puntos de igual temperatura. |
||
| U4: Electrostática | UNIDAD IV BASES FÍSICAS DE LOS FENÓMENOS BIOELÉCTRICOS
Electrostática - Campo Eléctrico Conceptos básicos
|
|
breve resumen de electroestática, y ejercitación (con las respuestas) |
||
| U4: Capacitores | Capacitores Asosiación en serie y en paralelo
|
|
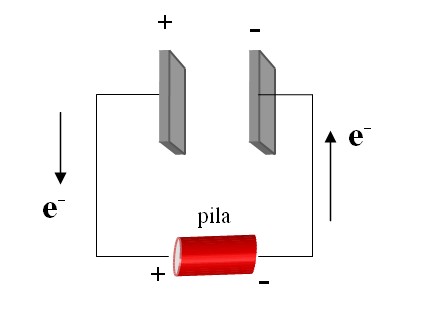
| U4: Electrodinámica |
Ley de Ohm Circuitos eléctricos
|
|
| Parciales para ejercitar (2°) | ||
| FINALES | ||