BIOFISICA | SILVA | S.ISIDRO-MI-SA:7-13hs 1 ° cuatr. 2026
Perfilado de sección
-
UNIDAD III
LA TERMODINÁMICA EN LOS SERES VIVOS- En el siguiente cuadro seleccionamos una serie de videos de la cátedra de calorimetría.
- Te indicamos las páginas que deberías leer para acompañar la practica. (ver apunte oficial de termodinámica)
- y en ejercitación relacionada a este tema. Fíjate que en este caso la ejercitación esta dividida en dos secciones: los ejercicios de desarrollo y los de elección múltiple (ver la guía de problemas)
- Al final de la sección algunos apuntes adicionales del temas, teóricos, prácticos y de ejercitación)
-
 Las mezclas con cambios de estado introducen un nivel de dificultad considerable. Solamente la práctica nos hará efectivos en la resolución de estos problemas. Veamos como nos desempeñamos en un ejemplo en donde la variación de una de las variables involucradas conduce a diferentes resultados.
Las mezclas con cambios de estado introducen un nivel de dificultad considerable. Solamente la práctica nos hará efectivos en la resolución de estos problemas. Veamos como nos desempeñamos en un ejemplo en donde la variación de una de las variables involucradas conduce a diferentes resultados. -
El punto de fusión es la temperatura a la que una sustancia en estado sólido se transforma en estado líquido. Por el contrario, el punto de solidificación, también conocido como punto de congelación, es la temperatura a la que un líquido se convierte en sólido. Y esto cambia en fusión de la presion atmosférica.
En el siguiente diagrama de fases del agua, vemos por ejemplo que a 1 atmosfera, el punto de fusión (o de solidificación) es a 0 °C. El punto de ebullición es la temperatura a la que un líquido se convierte en gas, mientras que el punto de condensación es la temperatura a la que un gas se convierte en líquido. A 1 atmosfera, el punto de ebullición (o de condensación) e100 a 0 °C.
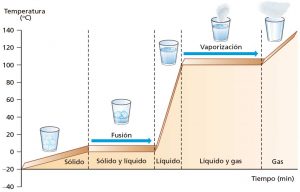
El agua puede cambiar de estado (sólido, líquido, gaseoso) a través de diferentes procesos como la fusión (sólido a líquido), la solidificación (líquido a sólido), la vaporización (líquido a gaseoso), la condensación (gaseoso a líquido), la sublimación (sólido a gaseoso) y la de sublimación (gaseoso a sólido).
El agua es el único componente de la Tierra que puede encontrarse en tres estados físicos: sólido, líquido y gaseoso.

El calor específico del agua es la cantidad de calor necesaria para elevar la temperatura de 1 gramo de agua en 1 grado Celsius. El calor latente del agua, por otro lado, es la cantidad de calor necesaria para cambiar el estado del agua de un estado a otro sin cambiar su temperatura.
El calor específico del hielo es 0.5 cal/g·°C, el del agua es 1 cal/g·°C y el del vapor de agua es aproximadamente 0.48 cal/g·°C.
Los cambios de estado se realizan a temperatura constante. Se necesitan 80 cal/g para derretir hielo (o congelarlo) y 540 cal/g para evaporar (o condensar). A lo largo de los cambios de estado, o transiciones de fases coexisten ambas fases, la materia en ambos estados.